オレキシン産生神経特異的にCreリコンビナーゼを発現するマウスの作製
発表者:平島 範子 指導教官:三輪 佳宏
導入・目的オレキシンA及びBは、オーファン受容体の内因性リガンドとして同定された神経ペプチドであり、共通の前駆体であるプレプロオレキシンから生成される。その受容体は、OX1及びOX2という、アミノ酸レベルで64%の相同性をもつ2種類のG蛋白質共役型受容体が見出されている。OX1受容体はオレキシンAに選択的だが、OX2受容体はオレキシンA、Bに同程度の親和性を持つ。プレプロオレキシンとその受容体は全て脳特異的に発現している。特にプレプロオレキシンは摂食中枢として知られていた視床下部外側野(LHA)と、その周辺の特定のニューロンに特異的に発現していたことから、摂食行動への関与が示唆された。実際、オレキシンの脳室内投与により摂食量が用量依存的に増加することが認められた。 1994年のレプチンの発見により、その主要な作用部位である視床下部においての神経伝達機構が分子レベルで明らかにされてきた。レプチンは脂肪組織から循環血液中に分泌されるホルモンで、摂食量を抑制し、エネルギー消費を亢進させ、最終的には体重を減少させる。 オレキシン産生神経の約半分はレプチン受容体を発現している。ラットにおいてレプチンを投与すると、絶食時に起こるオレキシンmRNAレベルの上昇が抑制されることから、オレキシン産生神経はレプチンによる抑制を受けていると考えられる。 そこで本研究では、レプチン受容体(OB-Rb)の下流で働く転写因子STAT3の遺伝子が、オレキシン産生神経特異的にノックアウトされるマウスを確立し、オレキシン神経におけるレプチンからのシグナルを遮断することによって、レプチンとオレキシンの関係を解析する。 実験方法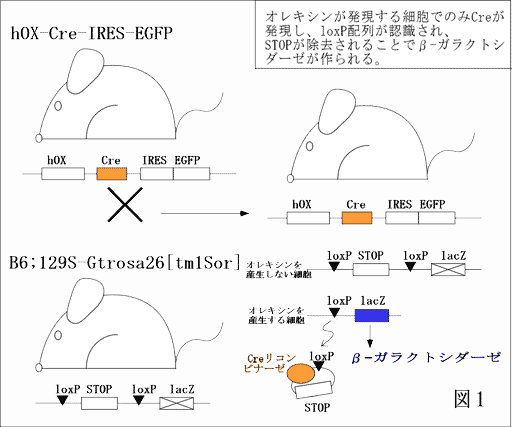
結果現在、二重免疫染色によってオレキシン産生神経におけるCreリコンビナーゼの発現率を解析している。また、X-galの染色により、オレキシン産生神経でのみCre-loxP系が働いているかどうかを確認しているところである。今後の展開レプチン受容体の下流で機能する転写因子STAT3のエクソン22をCreリコンビナーゼの認識配列ではさんだマウス(floxed-Stat3)と、hOX-Cre-IRES-EGFPマウスをかけ合わせ、レプチンのオレキシン産生神経への影響を解析してゆく予定である。 |