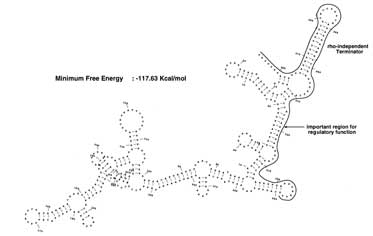
Fig1. VR-RNAの予測二次構造
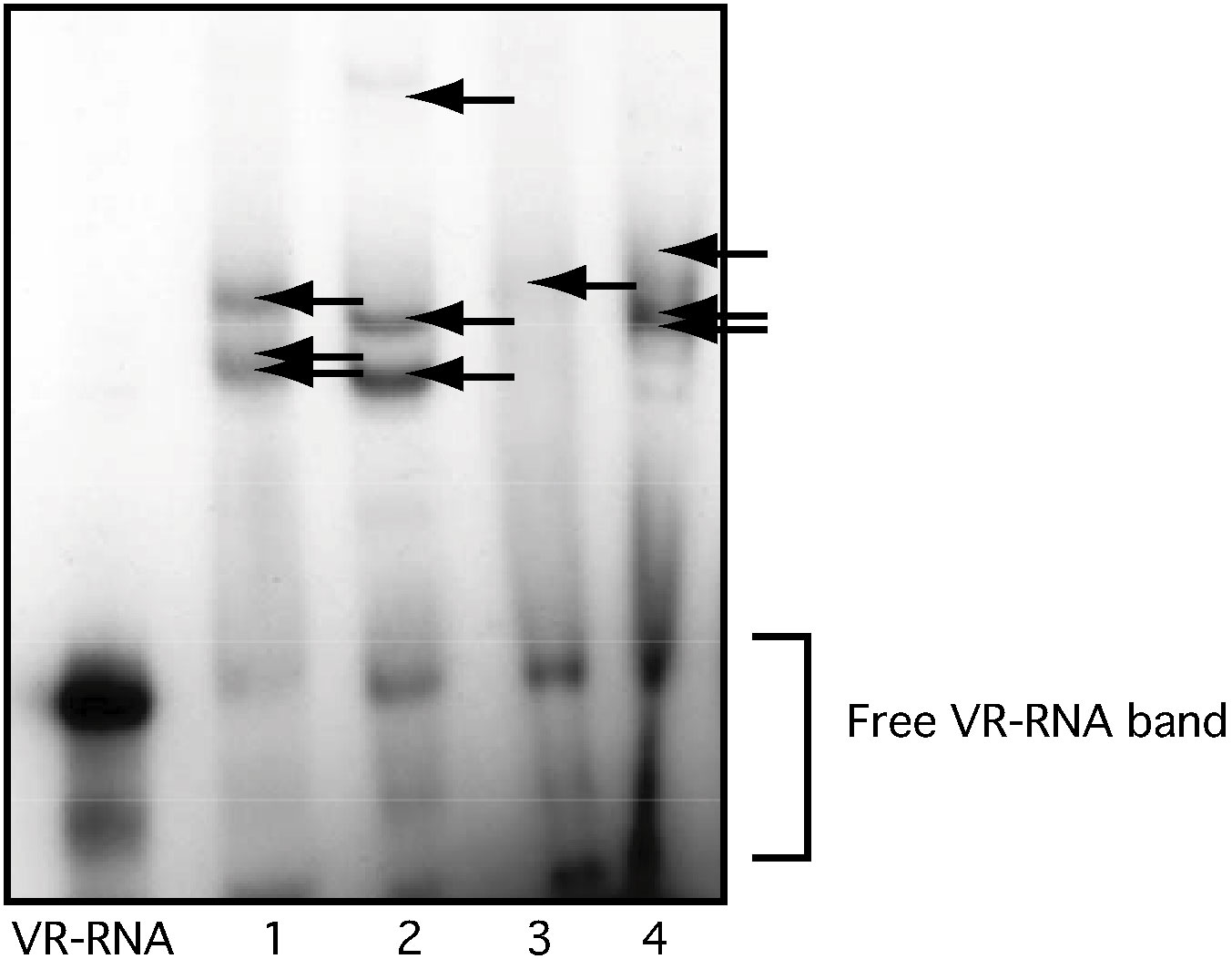
Fig2. ウェルシュ菌ライゼートに対してVR-RNAをprobeに用いたgel shift assay
(シフトバンドを矢印で示す, lane1: total lysate,2: 硫安0-30%, 3:30-60%, 4:60%<)
工藤 稚子 (筑波大学 生物学類 4年) 指導教官: 中村 幸治 (筑波大学 生物科学系)
VR-RNA結合タンパク質の探索:ウェルシュ菌野生株( strain13) にクロラムフェニコール耐性のpJIR418プラスミドを導入した株をクロラムフェニコール存在下において37℃で培養し、細胞抽出液を調製した。細胞抽出液を硫安分画により3段階のフラクションに分け、VR-RNA(Fig1)をプローブとしてゲルシフトアッセイによる結合タンパク質の探索を行った。
VR-RNA制御下にあるタンパク質の網羅的解析:ウェルシュ菌野生株(strain13)とVR-RNA遺伝子破壊株(TS140)にクロラムフェニコール耐性のpJIR418プラスミドを導入した株を、各々結合タンパク質探索の場合と同様の条件で細胞抽出液を調製した。次に、両者の細胞抽出液をAmersham bioscience社2D fraction kitにより6段階に分画し、それぞれのフラクションに対して二次元電気泳動を行った。さらに、発現に差異のあったスポットについてN末端解析によるタンパク質の同定を行った。
結合タンパク質の探索:ゲルシフトアッセイをおこなった結果、全てのフラクションにおいてシフトバンドが得られた(Fig2)。各フラクションにおいてシフトパターンの異なるバンドが複数得られ、バンドの濃さも各バンドによりそれぞれ異なっていた。従って、ウェルシュ菌では少なくとも数種類のVR-RNA結合タンパク質が存在することが明らかになった。また、泳動の結果、硫安濃度が30%以上のレーンになると、フラクション中に含まれるタンパク質量が多く、ゲルシフトアッセイにおいて複数のバンドが重なって一つのバンドに写ってしまっていた(Fig2 lane3, 4)。従って、今後、各フラクションサンプルについてさらに分画を行い、より詳細な解析を行っていくことが必要であるといえる。
VR-RNA制御下にあるタンパク質の網羅的探索:strain13株及びTS140株のライゼートを分画後、濃度測定及びSDS-PAGE電気泳動を行い、分画後における各フラクションのタンパク質含有量を調べた。二次元電気泳動の結果、fraction6ではタンパク質がほとんど存在しないことが明らかになったため、fraction1-5のサンプルに関して二次元電気泳動を行った。その結果、strain13株とTS140株において差異のあるスポットがいくつかのフラクションで確認され、特にfraction4において最も明瞭なスポットが得られたため、ゲルをメンブレンに転写後、泳動の結果からfraction4で差異のあったスポットについてN末端解析を行いタンパク質同定を行った。

Fig1. VR-RNAの予測二次構造 |

Fig2. ウェルシュ菌ライゼートに対してVR-RNAをprobeに用いたgel shift assay (シフトバンドを矢印で示す, lane1: total lysate,2: 硫安0-30%, 3:30-60%, 4:60%<) |