|
偮偔偽惗暔僕儍乕僫儖丂Tsukuba Journal of Biology (2006) 5: TJB200605SE2.
僸僩偺帯椕傊岦偗偰
乣惗暔妛椶惗偨偪偑偙偠奐偗偨儈僩僐儞僪儕傾昦堚揱巕帯椕傊偺摴乣
TJB妛惗曇廤晹 乮拀攇戝妛丂惗暔妛椶乯
丂儈僩僐儞僪儕傾丅巹偨偪偺嵶朎偺拞偵偁傝丄屇媧傪偮偐偝偳傞嵶朎彫婍姱偱丄媥傓偙偲側偔惗柦妶摦偵昁梫側僄僱儖僊乕傪惗傒弌偟偰偄傞丅1偮偺嵶朎撪偵悢昐屄傕懚嵼偟丄偦傟偧傟偑妀偲偼暿偵撈帺偺DNA乮儈僩僐儞僪儕傾DNA乯傪帩偭偰偄傞丅偝傜偵儈僩僐儞僪儕傾娫偵偼屳偄偵嶌傝弌偟偨暔幙傪岎姺偡傞偙偲偑偱偒傞傛偆側憡屳嶌梡偑懚嵼偡傞丅傕偟丄儈僩僐儞僪儕傾DNA偵曄堎偑拁愊偟偰儈僩僐儞僪儕傾偺屇媧婡擻偑惓忢偵偼偨傜偐側偔側傟偽丄惗懚偵昁梫側僄僱儖僊乕偑晄懌偟丄曄堎偺検偑偁傞堦掕抣傪挻偊偨偲偒丄乽儈僩僐儞僪儕傾昦乿偲屇偽傟傞幘姵偵側傞丅
丂儈僩僐儞僪儕傾昦偼丄儈僩僐儞僪儕傾偺屇媧妶惈偑壓偑傞偙偲偱敪昦偡傞丅僸僩偑偙偺昦婥偵偐偐傞偲丄抦擻掅壓丒彫擼幐挷丒嬝椡掅壓丒偗偄傟傫丒擄挳偲偄偭偨徢忬偑傒傜傟傞傛偆偵側傞丅崱傑偱偼帯椕朄偺側偄昦偱偁偭偨丅
丂2000擭丄杮妛戝妛堾惗柦娐嫬壢妛尋媶壢偺椦弮堦嫵庼偼丄悽奅偱弶傔偰儈僩僐儞僪儕傾昦儌僨儖儅僂僗乽儈僩儅僂僗乿傪嶌惢丅2005擭偵偼儈僩儅僂僗偵懳偡傞堚揱巕帯椕偵惉岟偟丄擄昦偺崕暈偵岦偗偰戝偒側堦曕傪摜傒弌偟偨丅挿擭儈僩僐儞僪儕傾尋媶傪懕偗偰偙傜傟偨椦嫵庼偵丄尋媶偵偮偄偰丄傑偨崱屻偺書晧偵偮偄偰偍榖傪偆偐偑偭偨丅乮TJB妛惗曇廤晹乯

儈僩儅僂僗丅儅僂僗偑儈僩僐儞僪儕傾昦偵偐偐傞偲丄怱揱摫忈奞丒掅恎挿丒掅懱廳丒嬝擏堎忢丒恡旍戝偲偄偭偨奜尒揑側徢忬偑傒傜傟傞丅
TJB乗乗儈僩僐儞僪儕傾昦偺尋媶偺宱堒傪嫵偊偰偔偩偝偄丅
椦乗乗巹偼拀攇戝妛偵晪擟偡傞慜丄嶉嬍導棫偑傫僙儞僞乕偵嬑傔偰偄傑偟偨丅偦偺崰偺尋媶僥乕儅偼丄偑傫乮庮釃乯偲儈僩僐儞僪儕傾DNA偲偺娭學偱偟偨丅惓忢嵶朎偲偑傫嵶朎娫偱儈僩僐儞僪儕傾DNA
傪岎姺偡傞幚尡傪峴偭偨寢壥偐傜丄椉幰偺娫偵場壥娭學偑懚嵼偟側偄偙偲傪柧傜偐偵偟傑偟偨丅偟偐偟摉帪丄儈僩僐儞僪儕傾DNA偺撍慠曄堎偼偑傫偱偼側偔儈僩僐儞僪儕傾昦偺尨場偵側傞偙偲偑媈傢傟傞傛偆偵側傝丄儈僩僐儞僪儕傾昦偺側偐偵儈僩僐儞僪儕傾DNA偲摨偠偔曣惈堚揱偡傞傕偺偑偁傞偲偄偆偙偲傕暘偐偭偰偒傑偟偨丅傕偟偐偟偨傜丄儈僩僐儞僪儕傾DNA偲儈僩僐儞僪儕傾昦偼捈愙娭學偁傞偐傕偟傟側偄偲巚偄丄拀攇戝妛偵晪擟屻丄堄梸揑側惗暔妛椶惗偨偪偲偲傕偵尋媶偵偲傝偐偐傝傑偟偨丅
丂曣惈堚揱偡傞儈僩僐儞僪儕傾昦偑偁偭偰傕曣恊偺怘惗妶傗曣擕偐傜揱傢傞摍偺偄傠偄傠側壜擻惈偑偁傞偺偱丄杮摉偵儈僩僐儞僪儕傾DNA偺曄堎偑儈僩僐儞僪儕傾昦偵娭學偡傞偺偐偼暘偐傝傑偣傫偱偟偨丅捈愙偺徹嫆偑側偐偭偨偺偱偡丅
丂偁傞偲偒丄儈僩僐儞僪儕傾昦姵幰偺儈僩僐儞僪儕傾DNA偺側偐偵撍慠曄堎偑尒偮偐傝傑偟偨丅偦偙偱丄偙偺曄堎儈僩僐儞僪儕傾DNA傪丄傑偭偨偔儈僩僐儞僪儕傾DNA傪帩偨側偄傛偆偵張棟偟偨rho-0乮儘乕僛儘乯偲偄偆攟梴嵶朎偵擖傟偰屇媧妶惈傪傒傑偟偨丅幚尡偺寢壥丄曄堎儈僩僐儞僪儕傾DNA偺妱崌偑懡偔側傟偽側傞傎偳丄攟梴嵶朎偺屇媧妶惈偑壓偑傝傑偟偨丅偙偺寢壥偐傜丄乽偙偺曄堎儈僩僐儞僪儕傾DNA偑尨場偱屇媧妶惈偑掅壓偡傞乿偙偲偑妋偐傔傜傟偨偺偱偡丅偙偺庤朄偼嶉嬍導棫偑傫僙儞僞乕帪戙偵偑傫尋媶偱攟偭偨傕偺偱丄傛偆傗偔怴偟偄尋媶惉壥偵偮側偘傞偙偲偑偱偒傑偟偨丅
丂偙偙偱嵟傕廳梫側栤戣偼丄乽偙偺曄堎儈僩僐儞僪儕傾DNA偑尨場偱屇媧妶惈掅壓偡傞乿偲偟偰傕乽屇媧妶惈掅壓偑尨場偱儈僩僐儞僪儕傾昦偵側傞乿偺偐偲偄偆揰偱偡丅妀偑尨場偱昦婥偵側偭偰偄傞壜擻惈傪斲掕偟丄儈僩僐儞僪儕傾昦偲儈僩僐儞僪儕傾DNA偺曄堎偺場壥娭學傪挷傋傞偨傔偵丄妀偑傂偲傝傂偲傝堎側傞僸僩偱偼側偔丄儅僂僗傪巊偭偰尋媶傪恑傔傑偟偨丅幚尡偵梡偄傞儅僂僗偼嬤恊岎攝傪孞傝曉偟偰偄傞偨傔丄妀DNA偵屄懱嵎偑偁傝傑偣傫丅偦偙偱丄儈僩僐儞僪儕傾昦儌僨儖儅僂僗傪嶌惢偟偨偺偱偡丅妀偲堎側傝丄儈僩僐儞僪儕傾偵DNA
傪摫擖偡傞偙偲偼擄偟偄偺偱丄帺慠奅偐傜曄堎傪尒偮偗偰偙側偗傟偽側傝傑偣傫偱偟偨丅傑偨丄儈僩僐儞僪儕傾偼憡屳嶌梡偵傛偭偰偍屳偄偵懌傝側偄傕偺傪曗偄崌偆偺偱丄帩偮曄堎偑偡傋偰摨偠偱側偗傟偽屇媧妶惈偑壓偑傝傑偣傫丅惗暔妛椶惗偑峴偭偨懖嬈尋媶偺偍偐偘偱丄旕忢偵庤偺崬傫偩抧摴側嶌嬈傪捠偟偰丄傛偆傗偔儈僩僐儞僪儕傾昦儌僨儖儅僂僗乽儈僩儅僂僗乿偑偱偒偨偺偱偡丅
TJB乗乗儈僩儅僂僗嶌惢偱偼偳傫側偲偙傠偵嬯楯偟傑偟偨偐丅
椦乗乗撍慠曄堎傪婲偙偟丄偦傟偲傑偭偨偔摨偠曄堎傪帩偭偨儅僂僗傪惗傒弌偡偲偙傠偱偡丅崱夞梡偄偨曄堎儈僩僐儞僪儕傾DNA偼幚尡拞偵乽偙傟偼撍慠曄堎偩両乿偲婏愓揑偵尒偮偐偭偨傕偺偱偡丅崱偱偼巹偨偪偺尋媶幒偺拞偱丄曄堎傪嶌傝弌偡偨傔偺曽朄偑偒偪傫偲妋棫偟偰偄傑偡丅儈僩儅僂僗傪嶌偭偰5擭偑宱偪傑偡偑丄偄傑偩偵懠偺尋媶婡娭偐傜摨偠傛偆側儅僂僗偺嶌惢偵惉岟偟偨偲偄偆曬崘椺偼偁傝傑偣傫丅
TJB乗乗側偤儅僂僗偱尋媶偟傛偆偲巚偭偨偺偱偡偐丅
椦乗乗儅僂僗偺堦斣偺枺椡偼妀偺僶僢僋僌儔僂儞僪偑嬒堦偱偁傞偙偲偲丄僸僩偲摨偠歁擕椶偱偁傞偲偄偆揰偱偡丅儈僩僐儞僪儕傾DNA偑曄堎傪婲偙偟偨偲偒偵丄儅僂僗偺婄怓偵曄壔偑尰傟偨傝丄恔偊偨傝丄懠偵傕堎忢偑尒傜傟偨傝偟傑偡丅偦偺傛偆側応崌偵丄儅僂僗側傜夝朥偟偰憻婍傪娤嶡偡傞偙偲傕壜擻偱偡丅堦曽丄僸僩偑儈僩僐儞僪儕傾昦偵側偭偨偲偒偺庡側徢忬偼抦擻掅壓偱偡偐傜丄崱屻偺壽戣偼儈僩儅僂僗偱抦擻掅壓乮妛廗峴摦堎忢乯偑偍偙偭偰偄傞偙偲傪徹柧偡傞偙偲偱偡丅
丂傑偨丄儅僂僗偺妀偺僶僢僋僌儔僂儞僪偼丄堦棏惈偲摨偠掱搙偵嬒堦偱丄摨宯摑偱偁傟偽屄懱娫偱偺堘偄偑側偄偙偲傕尋媶偟傗偡偄梫場偺堦偮偱偡丅愭傎偳傕弎傋偨傛偆偵丄妀偺堘偄偑偁傞偲丄儈僩僐儞僪儕傾昦偺尨場偑儈僩僐儞僪儕傾DNA偺曄堎偺偣偄側偺偐丄妀DNA偺曄堎偑婲偙偭偰偄傞偣偄側偺偐敾暿偑擄偟偔側傝傑偡偑丄妀DNA偑摨堦偱偁傞偙偲偵傛傝丄偦偺傛偆側栤戣傪彍偔偙偲偑偱偒傑偟偨丅
TJB乗乗儈僩僐儞僪儕傾娫偺憡屳嶌梡偵偮偄偰暦偐偣偰偔偩偝偄丅
椦乗乗偙傟傕傗偼傝惗暔妛椶惗偵傛傞懖嬈尋媶偐傜偱偡偑丄儈僩僐儞僪儕傾偼偍屳偄偵梈崌偲暘棧傪孞傝曉偟偰偍傝丄偦偺嵺偵儈僩僐儞僪儕傾DNA偵懚嵼偡傞堚揱巕偺揮幨嶻暔傗東栿嶻暔傪岎姺偟偰偄傞偙偲偑柧傜偐偵側傝傑偟偨丅偱偡偐傜曄堎儈僩僐儞僪儕傾mtDNA偺妱崌偑偦傟傎偳懡偔側偄偆偪偼丄屇媧妶惈偼惓忢側抣偑曐偨傟傑偡丅傑偨丄栰惗宆偺儈僩僐儞僪儕傾DNA偼帺暘帺恎偺昁梫検偺2攞埲忋偺暔幙傪崌惉偟偰嫙媼偱偒傞偺偱丄儈僩僐儞僪儕傾DNA偵撍慠曄堎偑偁偭偨偲偟偰傕丄偦偺妱崌偑慡懱偺8乣9妱偵側傜側偄偲屇媧妶惈偼掅壓偟傑偣傫丅崌惉偝傟偨暔幙偼丄嵶朎撪偺偡傋偰偺儈僩僐儞僪儕傾偵嬒摍偵峴偒傢偨傝傑偡丅曄堎傪婲偙偟偨儈僩僐儞僪儕傾DNA偺妱崌偑9妱嬤偔偵側傞偲屇媧妶惈偼媫掅壓偟偰僛儘偵側傞偺偱偡偑丄偙傟偼奺儈僩僐儞僪儕傾偑屇媧妶惈傪堐帩偡傞偺偵昁梫側偩偗偺暔幙傪摼傜傟側偔側傞偐傜偱偡丅
TJB乗乗儈僩僐儞僪儕傾昦偺帯椕朄偵偮偄偰偍暦偐偣偔偩偝偄丅
椦乗乗変乆偼幚嵺偵儈僩儅僂僗偵懳偟偰庴惛棏堚揱巕帯椕傪峴偄傑偟偨丅偙偺尋媶傕惗暔妛椶惗偺懖嬈尋媶偑儀乕僗偵側偭偰偄傑偡丅傑偢峴偭偨偺偼嬌懱傪梡偄偨恌抐偱偡丅棏偑尭悢暘楐偺嵺偵曻弌偡傞嬌懱偼儈僩僐儞僪儕傾傪娷傫偱偄偰丄嬌懱偲庴惛棏偺曄堎儈僩僐儞僪儕傾DNA偺妱崌偼傎傏摨偠偱偡丅嬌懱傪庢傝弌偟丄曄堎儈僩僐儞僪儕傾DNA偺妱崌傪堚揱巕恌抐偱挷傋傑偡丅師偺恾偺傛偆偵儈僩僐儞僪儕傾DNA偼曣恊偐傜偺傒師悽戙偵揱傢傝傑偡丅偮傑傝丄儈僩僐儞僪儕傾昦傕曣惈堚揱偡傞偺偱丄曣恊偑儈僩僐儞僪儕傾昦偩偲巕偳傕傕昦婥偵側傝傑偡丅儈僩僐儞僪儕傾DNA偵曄堎偑偁傟偽丄曣恊偺庴惛棏偐傜妀傪庢傝弌偟偰丄妀傪彍偄偨寬峃側戞嶰幰偺枹庴惛棏偵堏怉偟傑偡丅偙偆偡傞偲丄帺暘偺巕偳傕偼昁偢昦婥偵側傞偲偄偆塣柦傪攚晧偭偨曣恊偐傜傕丄妀DNA偼椉恊偐傜傕傜偄丄儈僩僐儞僪儕傾DNA偩偗戞嶰幰偺傕偺傪帩偮丄昦婥傪帩偨側偄巕偳傕偑惗傑傟傞偺偱偡丅
丂幚偼妀堏怉偺嵺偵丄曣恊桼棃偺曄堎儈僩僐儞僪儕傾DNA偑傢偢偐偵堦弿偵堏怉偝傟偰偟傑偄傑偡丅偟偐偟丄堏怉屻偼庴惛棏撪偺儈僩僐儞僪儕傾偺戝敿偼戞嶰幰偺惓忢側傕偺偱偡丅儈僩僐儞僪儕傾DNA偼慻姺偊傪婲偙偝側偄偟丄傢偢偐側曄堎側傜憡屳嶌梡偱僇僶乕偝傟傑偡丅
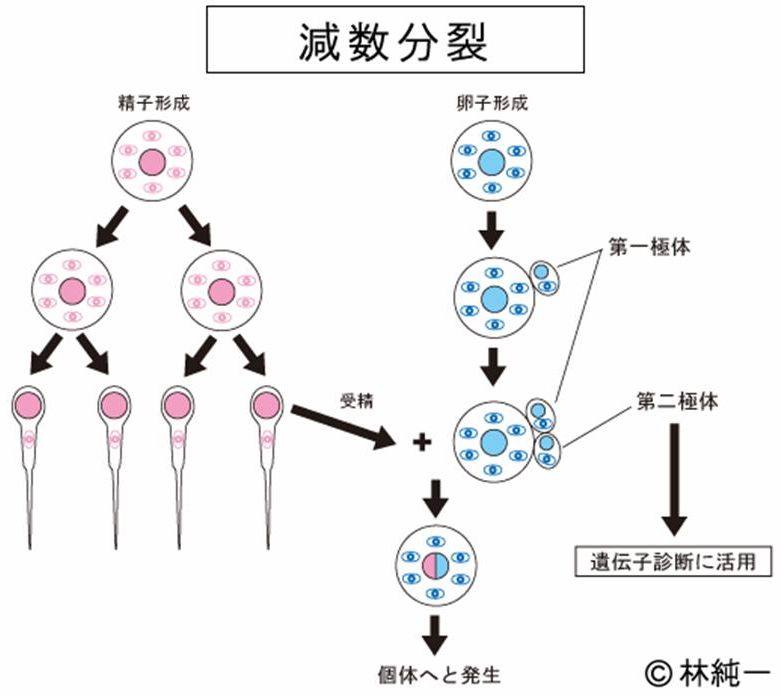
惛巕丒棏宍惉偵偍偗傞尭悢暘楐丅棏宍惉帪偵嬌懱偑攔弌偝傟傞丅庴惛偵傛偭偰妀偼椉恊偐傜敿暘偢偮庴偗宲偖偑丄儈僩僐儞僪儕傾DNA偼曣恊偐傜偺傒師悽戙偵揱傢傞丅
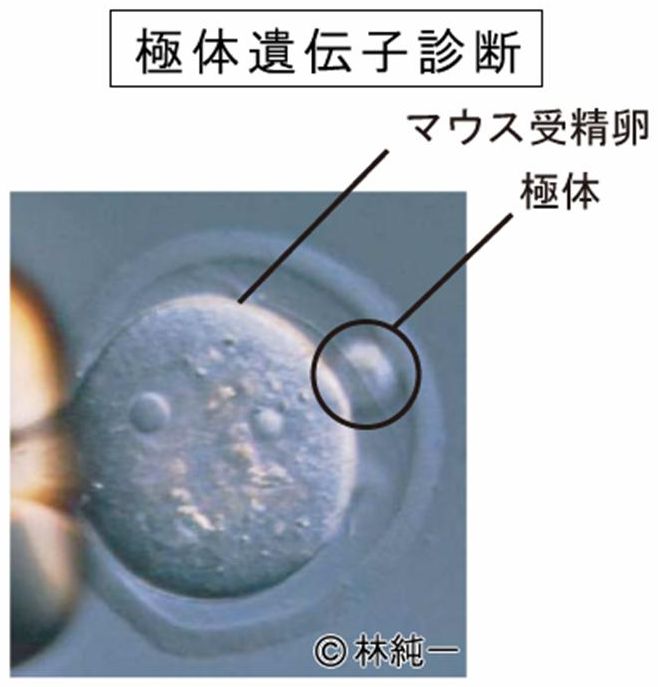
嬌懱堚揱巕恌抐丅尠旝嬀壓偱庴惛棏偐傜嬌懱偩偗傪庢傝弌偟丄堚揱巕恌抐偵傛傝儈僩僐儞僪儕傾DNA偺曄堎検傪挷傋傞丅
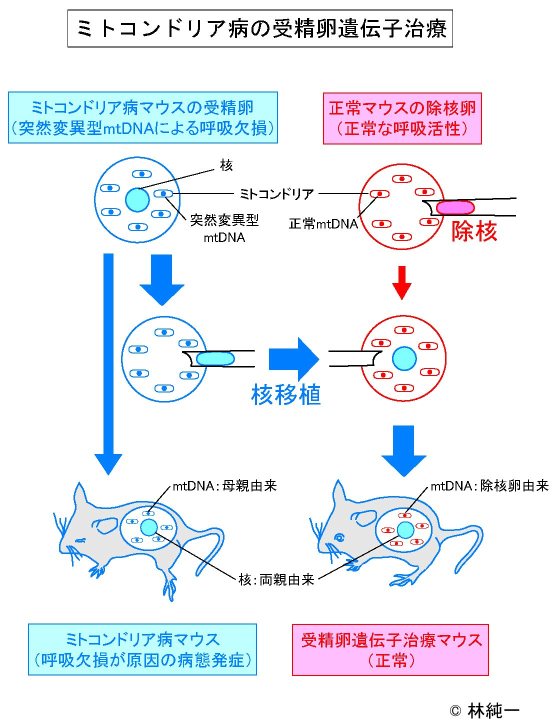
儈僩僐儞僪儕傾昦偺庴惛棏堚揱巕帯椕丅儈僩僐儞僪儕傾昦偺儅僂僗偺庴惛棏偐傜妀傪庢傝弌偟丄彍妀偟偨惓忢側儅僂僗偺枹庴惛棏偵堏怉偡傞偲丄惗傑傟偰偔傞儅僂僗偼惓忢側屄懱偲側傞丅
TJB乗乗崱屻偺尋媶偵偮偄偰嫵偊偰偔偩偝偄丅
椦乗乗傑偢1偮偼丄懠偺庬椶偺曄堎儈僩僐儞僪儕傾DNA傪帩偭偨儅僂僗傪嶌傝弌偡偙偲偱偡丅崱傑偱偵丄儈僩僐儞僪儕傾DNA偺堦晹偺墫婎攝楍傪幐偭偨寚幐撍慠曄堎傪帩偭偨儌僨儖傪嶌傝傑偟偨丅偟偐偟丄堎側傞庬椶偺堚揱巕偵堎側傞庬椶偺撍慠曄堎偑惗偠傞偙偲偵傛傝丄屇媧妶惈偺壓偑傝曽偼堎側偭偰偒傑偡丅儈僩僐儞僪儕傾昦偑敪昦偟偨嵺偺椪彴徢忬乮昞尰宆乯傕堎側偭偰偒傑偡丅偱偡偐傜丄崱偼暿偺曄堎傪擖傟偨儅僂僗偺嶌惢偵椼傫偱偄傞偲偙傠偱偡丅
丂2偮栚偵庢傝慻傫偱偄傞偙偲偼丄惉懱偵懳偡傞帯椕朄偺奐敪偱偡丅庴惛棏帯椕偺惉岟偱丄尰嵼儈僩僐儞僪儕傾昦偵側偭偰偄傞悽戙偺師偺悽戙偑儈僩僐儞僪儕傾昦偵側傞偙偲傪杊偖偙偲偼偱偒傞傛偆偵側傝傑偟偨丅偟偐偟丄崱丄儈僩僐儞僪儕傾昦偱偁傞恖偵懳偡傞桳岠側帯椕朄偼尒偮偐偭偰偄傑偣傫丅偙偙偱拲栚偟偨偺偑丄崪悜姴嵶朎偺拞偵偼偁傜備傞庬椶偺嵶朎偵暘壔偱偒傞擻椡偱偁傞乽慡擻惈乿傪帩偭偨嵶朎偑偁傝丄偦傟偑懱拞傪弰偭偰椺偊偽恄宱姴嵶朎偵側傝恄宱暘壔偵娭傢偭偰偄傞偲偄偆壜擻惈偱偡丅偦偙偱儈僩僐儞僪儕傾昦偵側偭偨儈僩儅僂僗偺寣塼拞偱崪悜姴嵶朎偑惓忢側慻怐偺姴嵶朎偵暘壔偟丄偝傜偵偦偙偐傜惓忢側嵶朎偑嶌傜傟傞偺偱偼側偄偐偲峫偊偨偺偱偡丅敀寣昦帯椕偲摨偠傛偆偵丄儈僩儅僂僗偺崪悜偵X慄徠幩偟偰崪悜嵶朎傪彍嫀偟丄惓忢側儈僩僐儞僪儕傾DNA傪帩偮崪悜姴嵶朎傪堏怉偟傑偟偨丅偡傞偲丄寣塼嵶朎偺儈僩僐儞僪儕傾DNA偼姰慡偵抲偒姺傢傝丄庻柦傕堏怉傪偟側偄応崌傛傝傕丄栺4廡娫墑傃傑偟偨丅尰嵼偙偺曽朄偺夵椙傪恑傔偰偄傑偡丅
丂嬤擭丄儈僩僐儞僪儕傾DNA 偺曄堎偑榁壔傗偑傫壔偵傕娭傢偭偰偄傞傜偟偄偙偲偑懡偔偺尋媶幰偵傛偭偰曬崘偝傟偰偄傑偡偑丄偙偺栤戣偵傕寛拝傪拝偗偨偄偲巚偭偰偄傑偡丅

椦弮堦乮偼傗偟丒偠傘傫偄偪乯
拀攇戝妛戝妛堾惗柦娐嫬壢妛尋媶壢忣曬惗暔壢妛愱峌嫵庼丅摨戝妛戞擇妛孮挿丅
惗暔妛椶偱偼敪惗妛奣榑丄敪惗妛嘥丄憤崌壢栚乮堚揱巕偑偮偔傞暥柧乯側偳偺島媊傪扴摉丅挊彂偱偁傞儈僩僐儞僪儕傾偺僟僀僫儈僢僋側摦懺傪婰偟偨乽儈僩僐儞僪儕傾丒儈僗僥儕乕乿乮2002擭丂島択幮姧乯偼2003擭偵島択幮壢妛弌斉徿傪庴徿偟偨丅
Communicated by Jun-Ichi Hayashi, Received June 13, 2006.
©2006 拀攇戝妛惗暔妛椶
|