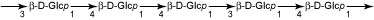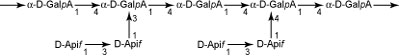|
生殖細胞など一時的な例外を除き、陸上植物の細胞は細胞壁 (cell wall) で囲まれている。ただし隣接する細胞の間は原形質連絡でつながっており、細胞壁は細胞間を完全に仕切っているわけではない。細胞壁の存在は、陸上植物と多細胞動物の間の大きな違いの1つであり、植物細胞の成長をコントロールすることを通じで組織、器官、そして植物体全体の形態形成に大きく関わっている。
陸上植物の細胞壁は、セルロースからなる基本骨格が他の多糖やタンパク質からなる基質(マトリックス matrix、基質ゲル matrix gel)の中に埋め込まれている。基質を構成する多糖は、伝統的に熱水や酸性緩衝液で抽出されるペクチン(pectin)と、アルカリに可溶な成分であるヘミセルロース(hemicellulose)に分けられているが、最近ではマトリックス多糖 (matrix polysaccharide) としてまとめられることが多い。
多くの被子植物の細胞壁はタイプ I とよばれ、セルロースとキシログルカンが多く、ペクチン、アラビノキシラン、 グルコマンナン、ガラクトグルコマンナンなどが含まれる。一方、単子葉類の一部(イネ目)の細胞壁はタイプ II とよばれ、セルロースとキシラン(グルクロノアラビノキシラン)、1,3-1,4-β-D-グルカンが多く、ペクチンやキシログルカンが少ない。またタイプ I の細胞壁では、構造タンパク質(エクステンシンなど)が大きな役割を果たしているが、タイプ II 細胞壁ではタンパク質含量が低く、フェノール酸(フェルラ酸など)の架橋がその代わりを果たしている。
細胞壁は細胞自体から遊離した存在ではない。少なくとも2つの構造で細胞壁最内層と細胞膜は架橋されている。1つは細胞膜に埋め込まれたセルロース合成酵素複合体から生じたセルロース繊維であり (下記参照)、もう1つは膜貫通タンパク質を介した細胞質表層微小管と細胞壁タンパク質の連絡である (下記参照)。おそらくこれらの架橋を通じて、原形質-細胞膜と細胞膜は相互作用している。
|
|
 セルロース セルロース
セルロース (cellulose) は、数千~数万の β-D-グルコース残基(グルコピラノース残基)が (1→4) グリコシド結合によって重合した直鎖状の高分子、つまり (1,4)-β-D-グルカンである (図1B)。
セルロースに限らず生体内のグルコース分子はすべて、立体配座としてイス型をとる。またセルロース分子ではこのイス型グルコースは、すべて4C1型である。セルロース分子内ではグルコース残基のO-6位とO-2位、O-3位とO-1位が水素結合によって結びつき、分子がねじれにくくさらに強固になっている (図1B)。セルロース分子の重合度は2,000~15,000ほどに達する。ただし長さ、重合度は生物種や組織、成長段階、環境によって変異がある (表1)。
細胞壁において、セルロース分子は数十本が平行に配列している。このとき隣接する分子間では、O-6位とO-3位の間で水素結合が形成され、直径3~4 nmほどの強固な束を形成している (図1B)。この束はエレメンタリーフィブリル(基本繊維 elementary fibril)とよばれ、さらにこれが数~数十本束になって直径数~20 nm、長さ 1~数 µmほどのセルロース微小繊維(ミクロフィブリル microfibril)を形成している。
セルロース微小繊維におけるセルロース分子のならび方には2つのタイプが見られる。セルロース I では全てのセルロース分子が同じ方向を向いているが、セルロース II ではミクロフィブリル中央のセルロース分子のみが反対方向に配向している。セルロース IIの方がエネルギー的に安定であるので、セルロースIの分子を分解して再構成させるとセルロース IIになってしまう。しかし陸上植物も含めて生物のつくるセルロースミクロフィブリルは全てセルロース Iである。これは生物におけるセルロース微小繊維の合成方法に起因している (後述参照)。セルロースIの中にもセルロース分子の並び方に変位が見られ、陸上植物ではおもにセルロース Iβ (単斜晶)を主成分とし、セルロース Iα (三斜晶)を含む (図1A)。
セルロ-ス微小繊維は、一次壁ではふつう細胞長軸に対して直角に配向しているが、細胞の成長に伴って変化する。一方、二次壁ではセルロ-ス微小繊維が直角、平行、直角と3層に列んでいることが多い。一次壁ではセルロース含量は20~40%、セルロース分子量は8万~100万程度であるが、二次壁ではセルロース含量が50~60%と多く、各セルロース分子量も120万~220万ほどであることが多い。
|
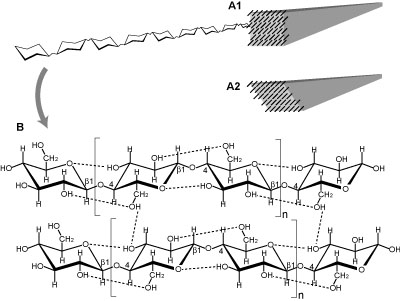
図1. セルロース. A. セルロースのエレメンタリーフィブリル. A1. セルロース Iα. A2. セルロース Iβ. B. セルロース2分子の構造. 点線は水素結合を示す。
| | ミクロフィブリルの幅 (nm) | セルロース重合度 |
| 一次細胞壁 | 2~2.5 | 2,00~6,000 (ワタ) |
| 二次細胞壁 | 5~10 | 13,000~14,000 (ワタ) |
| 木本形成層 | 1.5 | |
| 材 | | 8,200 |
| Valonia (アオサ藻) | 25~30 | 26,500 |
| Acetobacter (真正細菌) | 6 | 5,700 |
表1. さまざまな生物のミクロフィブリルの幅とセルロース重合度
|
 ヘミセルロース ヘミセルロース
細胞壁多糖類からペクチンを抽出した後に、アルカリで抽出される多糖類の総称がヘミセルロース (hemicellulose) である。水に不溶なものをヘミセルロースA、水溶性のものをヘミセルロースBとしたり、希薄なアルカリ (4%) に溶解するものをヘミセルロース I、濃アルカリ (24%) に溶けるものをヘミセルロース II とすることもある。ヘミセルロースには以下のようにさまざまなものが知られるが、多くの被子植物ではキシログルカン、イネ目ではキシラン (グルクロノアラビノキシラン) や 1,3-1,4-β-D-グルカンがそれぞれ主である。また裸子植物の二次壁やシダ植物ではグルコマンナンが多い。
キシログルカンやキシラン、β-1,3-β-1,4-グルカンはセルロースと水素結合しており、網状構造を形成している。この網状構造は酵素によって常時切断、再架橋が起こり、動的な状態にある。このような動的状態は細胞の伸張成長に大きく関わっている。またアラビノキシランなどではエステル結合したフェノール酸を介して互いに結合して細胞壁の強度を増している。
- キシログルカン (xyloglucan)
- 1,4-β-D-グルカンを主鎖とし、その多く (75%) のD-グルコース残基のO-6位にα-D-キシロース残基が結合している。α-D-キシロース残基には、β-D-ガラクトース残基やそれに加えてα-L-フコース残基がついていることがあり、またα-L-アラビノース残基がついていることもあるもある。D-グルコース残基は、これらの側鎖の種類からいくつかのタイプに分けられる (G, X, L, F, S, T, J) 。一般に被子植物には多く含まれ (一次壁で約20%) 、分岐度が約75%であり、容易に水に溶ける。イネ目には少なく (一次壁で約2%) 、分岐度が30~40%で水に不溶性なことが多い。キシログルカンは中葉を含めて細胞壁全体に分布し、セルロースに水素結合していると思われる。またキシログルカンは種子の貯蔵多糖として存在することもあり、アミロイドともよばれていた。
- 1,3-1,4-β-D-グルカン
- 単にβ-グルカン (β-glucan) とよばれることもある。β-D-グルコースが1,3または1,4結合してできている直鎖状多糖。1,3結合と1,4結合の比は種によって異なるが、一次壁では約30:70。基本的にセロトリオース (3糖の1,4-β-D-グルカン) やセロテトラオース (4糖の1,4-β-D-グルカン) の単位が、β-1,3結合で連なった分子である。イネ目植物に多く見られるが、その他の単子葉類や双子葉類にはほとんど存在しない。
- キシラン (xylan)
- β-D-キシロースが1,4結合してできている1,4-β-D-キシランを主鎖としている。側鎖をもたない純粋なキシランの場合もあるが、ふつうD-キシロース残基のO-3位にL-アラビノース残基が、O-2位に4-O-メチル-D-グルクロン酸残基またはD-グルクロン酸残基が結合している。そのほかにもO-3位にはさまざまな側鎖が知られている。
おもにβ-D-キシロースとD-グルクロン酸から構成されているものはグルクロノキシラン (glucuronoxylan) とよばれ、広葉樹に多く見られる。これに加えてL-アラビノースを多く含むものはグルクロノアラビノキシラン (glucuronoarabinoxylan) とよばれ、裸子植物やイネ目に多く見られる。またイネ目のキシラン (グルクロノアラビノキシラン) のL-アラビノース残基には、フェルラ酸やP-クマル酸がエステル結合していることがある。
- グルコマンナン (glucomannan)
- β-D-グルコースとβ-D-マンノースが1,4結合したものを主鎖とし、D-マンノース残基のO-6位にD-ガラクトース残基が、またO-2位やO-3位がアセチル化していることがある。D-グルコースとD-マンノースの割合はさまざまだが、ふつうD-マンノースの方が多い。裸子植物の二次壁やシダ植物に多い。またサトイモ科 (コンニャクイモなど) やラン科の根茎に貯蔵多糖として含まれることがある。
- カロース (callose)
- β-D-グルコースが1,3結合してできた1,3-β-D-グルカンである。水に不溶でアルカリに可溶。分子量は5万~20万。D-グルコース残基のO-6位にβ-D-グルコースがついていることもある。微量ではあるが広く分布しており、特に篩管や花粉管に存在し、また病原菌感染などの各種ストレスに対して生成される。特異な分布・挙動を示す多糖であり、ふつうヘミセルロースに含まれることはないが、便宜的にここに挙げた。
|
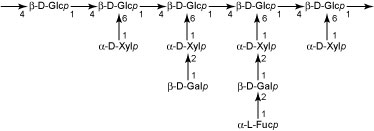
図2. キシログルカン.
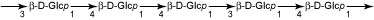
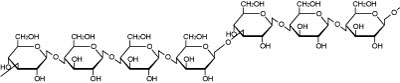
図3. 1,3-1,4-β-D-グルカン.
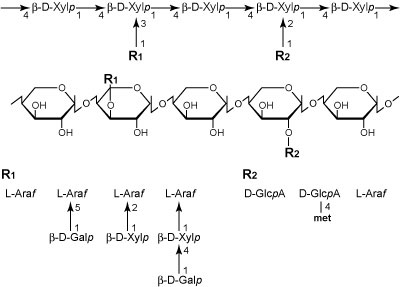
図4. キシランの主鎖と側鎖.
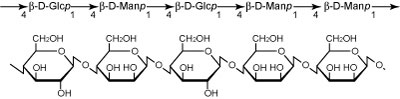
図5. グルコマンナン.
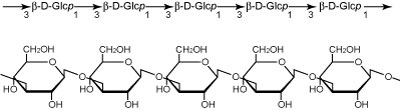
図6. カロース.
|
 ペクチン ペクチン
ペクチン (pectin) は、ペクチン質 (pectic substance) またはペクチン性多糖 (pectic polysaccharide) ともよばれる。細胞壁を熱水やキレート溶液で抽出して得られる酸性多糖の総称である。細胞壁においてペクチンは中葉に多く含まれ、細胞接着に大きな役割を果たしていると考えられている。またペクチンは、イネ科などを除き、一次壁にも多く含まれる。ペクチンには以下のようなものが知られるが、これらの多くはラムノガラクツロナン I を主とした巨大な分子を形成しているのかもしれない。
- ホモガラクツロナン (homogalacturonan, HG)
- D-ガラクツロン酸を主とする重合体、 (1,4) -α-D-ガラクツロナンであり、重合度は30以上。カルボキシル基がところどころでメチルエステル化している。ホモガラクツロナンはメチルエステル化していないカルボキシル基どうしが二価イオン (Caイオンなど) によってイオン結合してゲル化しており、細胞壁の構造保持に寄与している。
- ラムノガラクツロナン I (rhamnogalacturonan I, RG-I)
- D-ガラクツロン酸とL-ラムノースが交互に結合した4-D-ガラクトシルウロン酸ー2-L-ラムノシル (4-D-galactosyluronic acid-2-L-rhamnosyl) の重合体であり、少量のL-フコース残基 (L-fucosyl) を含んでいる。この主鎖におけるラムノシル残基の約半分のO-4位に、平均7個の糖残基からなる中性糖側鎖が結合している。側鎖の糖残基としてはL-ラムノース、D-ガラクトース、L-アラビノースが知られており、これらの数・組み合わせは30種以上に及ぶ。またガラクツロン酸残基に側差がついていることもある。平均重合度は約2,000。おそらくホモガラクツロナンと共有結合している。
- ラムノガラクツロナン II (rhamnogalacturonan II, RG-II)
- ホモガラクツロナンと同じく (1,4) -α-D-ガラクツロナンを主鎖とし (少なくとも8糖) 、そのO-2位またはO-3位に、L-ラムノース、L-アラビノース、D-アピオース、D-, L-ガラクトース、D-ガラクツロン酸、D-グルクロン酸、L-フコース残基、2-O-メチル-L-フコース残基、2-O-メチル-D-キシロース残基、アセリン酸 (aceric acid, 3-O-カルボキシ-5-デオキシ-L-キシロース) 残基、2-ケト-3-デオキシ-D-マンノ-2-オクツロン酸 (Kdo) 、3-デオキシ-D-リクソ-2-ヘプツロン酸 (Dha) からなる4種類の側鎖 (A, B, C, D) が結合している (図5) 。これらの糖の中にはRG-IIにしか見つかっていない特異なものがある。RG-IIもおそらくホモガラクツロナンと共有結合しており、またホウ素とエステル結合してダイマーを形成し細胞壁の安定化に寄与している。RG-IIは分解されにくいため、ワインなどにも多く含まれることが知られている (赤ワインで100-150 mg/l) 。
- アピオガラクツロナン (apiogalacturonan)
- (1,4) -α-D-ガラクツロナンのO-3位またはO-4位に、D-アピオースからなる2糖側鎖が結合したもの (図6) 。ウキクサ (サトイモ科) で見つかっている。
-
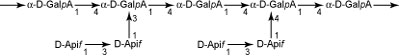
図6. アピオガラクツロナン.
-
- アラビノガラクタン (arabinogalactan)
- アラビノガラクタンはおもにアラビノース残基とガラクトース残基からなる多糖であり、大きく分けてタイプ I とタイプ II がある。タイプ I は1,4-β-D-ガラクタンを主鎖とし、一部のガラクトース残基の0-3位にアラビノフラノシル- (1,5) -アラビノフラノース残基が結合したものである。このタイプ I アラビノガラクタンはラムノガラクツロナン I の側鎖なのかもしれない。
タイプ II はアラビノ-3,6-ガラクタンともよばれ、 (1,3) -β-D-ガラクタンを主鎖とし、一部のガラクトース残基の0-6位にさまざまな糖残基が結合したものを基本構造としていると思われる。糖残基としてはL-アラビノース残基、アラビノピラノシル- (1,3) -アラビノフラノース残基、 (1,6) -β-D-ガラクタン (重合度1~30) などが知られている。またその他にL-フコース、L-ラムノース、D-マンノース、D-キシロース、D-グルコース、D-グルクロン酸、4-O-メチル-D-グルクロン酸、D-ガラクツロン酸、4-O-メチル-D-ガラクツロン酸などが含まれることがある。このタイプのアラビノガラクタンは、還元末端のD-ガラクトースとタンパク質のセリン残基がO-グリコシド結合して糖タンパク (アラビノガラクタンタンパク質) となっていることもある。アラビノガラクタンタンパク質は器官特異的であり、植物の分化と関連があるらしい。
- アラビナン (arabinan)
- アラバン (araban) ともよばれる。1,5-α-L-アラビナンを主鎖とし、ところどころのL-アラビノフラノース残基のO-3位またはO-2位に、α-L-アラビノフラノース残基が結合している中性多糖。
- ガラクタン (galactan)
- ふつう純粋な1,4-β-D-ガラクタンであるが、ときにO-6位で分岐しているものもある。
ペクチンは特異なゲル化能をもつため、食品工業などで利用されている。特にオレンジの果皮やイチゴの果実には多く含まれており、マーマレードやジャムとして食用にされる。このような分野では、ガラクツロン酸遊離のものをペクチン酸 (pectic acid) 、メチルエステル化されたものを水溶性に応じてペクチン (pectin) またはペクチニン酸 (pectinic acid) とよんでいる。
|
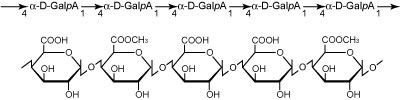
図2. ホモガラクツロナン.
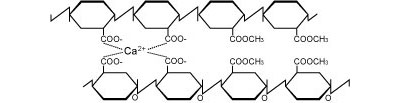
図3. ホモガラクツロナン分子間のカルシウムイオンによる架橋.
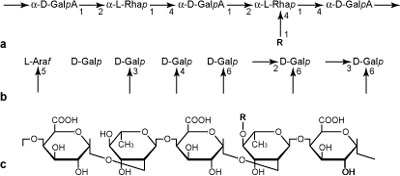
図4. ラムノガラクツロナン I. a. 主鎖. b. 側鎖の還元末端. c. 主鎖 (ハースの式) .
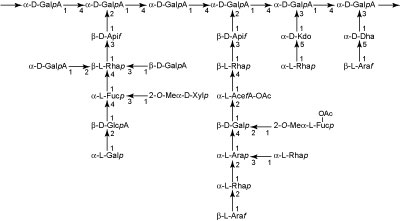
図5. ラムノガラクツロナン II.
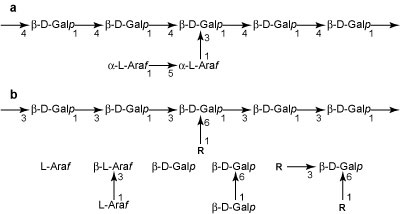
図7. アラビノガラクタン. a. タイプI. b. タイプII (アラビノ-3,6-ガラクタン) の主鎖と側鎖 (R) .

図8. アラビナン.
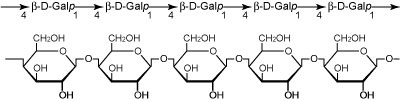
図9. ガラクタン.
|
 糖タンパク質 糖タンパク質
細胞壁にはさまざまな糖タンパク質 (glycoprotein) が存在し、構造タンパク質や細胞間認識物質として働いている。
エクステンシン (extensin, EXT) はシカモカエデ (ムクロジ科) の培養細胞から発見された細胞壁構造糖タンパク質であり、当初は細胞伸長に関与すると考えられたため、エクステンシンという名前が与えられた。しかし、その後このタンパク質は細胞伸長ではなく、むしろ細胞壁の強化・伸長抑制に働くことが明らかになっている。
エクステンシンのアミノ酸組成としてはヒドロキシプロリン (Hyp) の含量が非常に高く (25~50%) 、その他にセリン (10%) 、リジン (7~14%) 、チロシン (4~12%) 、ヒスチジン (3~11%) などが多い。リジン残基が多いため塩基性を示す。エクステンシンの糖含量は50%程度であり、ヒドロキシプロリン残基には1~4個のL-アラビノース残基からなる糖鎖が、またセリン残基には1個のα-D-ガラクトースが、それぞれO-グリコシド結合している。イネ類では糖側鎖が少ない。2分子のエクステンシンはチロシン残基どうしでイソジチロシン架橋を形成し、セルロースミクロフィブリルを挟み込んで固定していると考えられている。またエクステンシンは膜貫通型タンパク質を介して細胞表層微小管と連絡しており、その安定性に関与しているらしい。
アラビノガラクタンタンパク質 (arabinogalactan protein, AGP) はエクステンシンと似てヒドロキシプロリン含量が多いが、その他にセリン、アラニン、グリシンが多いため酸性を示す。そのセリン残基には、アラビノガラクタンの還元末端にあるD-ガラクトースがO-グリコシド結合している。エクステンシンとは異なり、糖の重合度が大きいため、糖含量は90%以上に達する。アラビノガラクタンタンパク質は細胞間認識に働いていることが知られており、導管分化に働くザイロゲンなどが知られる。
|
|
 フェノール化合物 フェノール化合物
陸上植物の細胞壁には、2種類のフェノール化合物が知られている。
1つは3種類のフェニルプロパノイド (phenylpropanoid I - III) が高度に脱水素重合して複雑な樹枝状構造をした物質であるリグニン (木質素 lignin) である。フェニルプロパノイドは細胞外へ放出され、細胞壁中で重合する。リグニンはふつう二次壁に多く含まれ、木材中の割合は20~30%に達する。リグニンはセルロースなどの多糖と結合して存在し、細胞壁の機械的強度を飛躍的に高くするとともに、細胞壁の化学的・生物学的抵抗性が高くなる。細胞壁にリグニンが蓄積されていく過程を木化 (リグニン化 lignification) とよぶ。リグニンはI型からIII型が知られるが、双子葉植物やマオウ類ではI, II型、イネ目ではI, II, III型が存在する。球果類はシナピン酸 (II型) 合成酵素を欠くため、I型のみをもつ。コケ植物にはリグニンは存在しない。リグニンはセルロースに次いで地球上に多い有機炭素化合物である。
2つめとして、フェニルプロパノイドの単量体がさまざまなマトリックス多糖の側鎖にエステル結合していることが知られている。
また細胞壁にはフェルラ酸 (ferulyl residue) など多くのフェノール酸が存在する。双子葉植物の細胞壁にも存在するが (250糖残基に1分子) 、特にイネ目の細胞壁 (タイプ II 細胞壁) には多い。
例えば、4-O- (6-O-フェルロイル-β-D-ガラクトピラノシル) -D-ガラクトピラノースや3-O- (3-O-フェルロイル-α-L-アラビノピラノシル) -L-アラビノピラノースは
イネ目の細胞壁に多く含まれ (細胞壁フェルラ酸の60~70%) 、キシラン (グルクロノアラビノキシラン) と結合している。
またO- (4-O-トランス-フェルロイル-α-D-キシロピラノシル) - (1→6) -D-グルコピラノースはキシログルカンに結合している。
ペクチンに存在し、ラムノガラクツロナン I、ガラクタン、アラビナンまたはアラビノガラクタンに結合した形で存在するものと思われる。
これらフェルラ酸エステル糖残基は、ペルオキシダーゼの働きで互いに結合してジフェルラ酸になることで多糖間の架橋を形成し、細胞壁の安定化、伸長阻止に寄与している。
|
|
 細胞壁酵素 細胞壁酵素
- ペルオキシダーゼ (peroxidase, EC 1.11.1.7)
- 細胞壁内にはイオン結合または共有結合、可溶性の形で存在する。シキミ酸経路やケイ皮酸経路でできたコニフェリルアルコール (coniferyl alchol) を、H2O2存在下の脱水素反応によって重合させて、二次壁の重要な成分であるリグニンを形成する。またアラビノガラクタンやキシログルカンに結合しているフェルラ酸やp-クマル酸の間のジフェルラ酸架橋の形成や、エクステンシンのチロシン残基間のイソジチロシン架橋の形成にも関わっている。
- リンゴ酸脱水素酵素 (malate dehydrogenase, EC 1.1.1.37)
- リグニン生成などペルオキシダーゼの反応にはH2O2が必要となるが、酸素からH2O2の生成に関与するNADHの供給にこの酵素が寄与している。また病原菌の感染に対する防御機構にも関与している。
- エンド-1,4-β-D-グルカナーゼ (endo-1,4-β-D-glucanase, EC 3.2.1.4)
- セルラーゼ (cellulase) ともよばれる。セルロースやキシログルカン、1,3-1,4-β-D-グルカン、グルコマンナンなどが基質となりうるが、主にキシログルカンを分解するらしい。
- エンド-1,3-β-D-グルカナーゼ (endo-1,3-β-D-glucanase, EC 3.2.1.6)
- カロースや1,3-1,4-β-D-グルカンの分解に関与しているものと思われる。
- α-D-マンノシダーゼ (α-D-mannosidase, EC 3.2.1.24)
- β-D-マンノシダーゼ (β-D-mannosidase, EC 3.2.1.25)
- β-D-グルコシダーゼ (β-D-glucosidase, EC 3.2.1.21)
- α-D-ガラクトシダーゼ (α-D-galactosidase, EC 3.2.1.22)
- β-D-キシロシダーゼ (β-D-xylosidase, EC 3.2.1.37)
- α-L-アラビノフラノシダーゼ (α-L-arabinofuranosidase, EC 3.2.1.55)
- β-D-グルクロニダーゼ (β-D-glucuronidase, EC 3.2.1.31)
- 上記のようなエキソ型分解酵素は、細胞壁の構成多糖のほか、糖タンパク質や糖脂質の糖鎖の代謝を関わっている。また病原菌の感染に対する防御機構にも関与している。
- ペクチナーゼ (pectinase, EC 3.2.1.15)
- ペクチンメチルエステルラーゼ (pectin methylecterase, EC 3.1.1.11)
- ポリガラクツロナーゼ (polygalacturonase, EC 3.2.1.15)
- ペクチンメチルエステルラーゼはエステル化されたカルボキシル基の部分を加水分解し、ポリガラクツロナーゼはガラクツロナンのエンド型分解酵素である。ともにペクチンの分解に関わっている。
|
|
 セルロース
セルロース